Bradfuteラボ

集団に新たに出現した、または存在したが発生率または地理的範囲が急速に増加している感染症/病原体

シロアシネズミPeromyscusmaniculatusは、米国のハンタウイルス心肺症候群のほとんどの症例の原因であるシンノンブルハンタウイルスを保有しています。
写真提供者:Sam Goodfellow

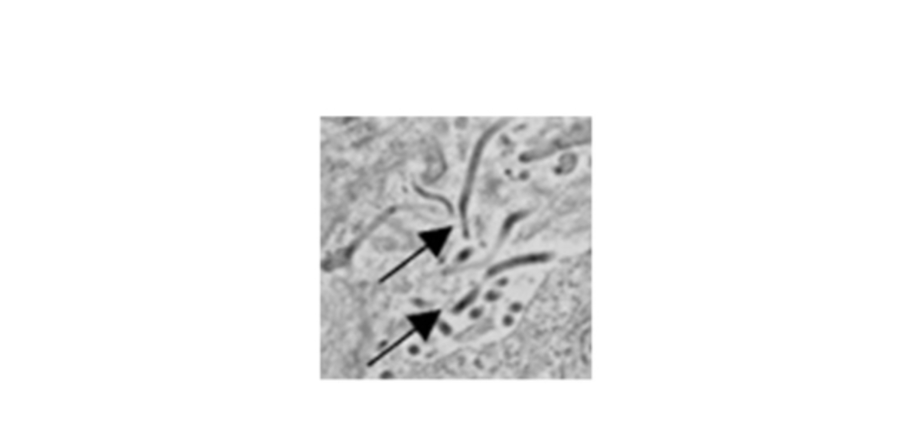
感染した脾臓のエボラウイルス。 矢印は個々のビリオンを指しています。 透過型電子顕微鏡を使用して実行されるイメージング。
写真提供者:Steven Bradfute、PhD

中和抗体を同定するためのジカウイルスプラークアッセイ
写真提供者:Steven Bradfute、PhD
エボラウイルス感染は免疫細胞の死を引き起こします。 蛍光顕微鏡は、感染した動物の脾臓細胞を示しています。 赤は死にかけている細胞を示し、すべての細胞を示しています。
写真提供者:Steven Bradfute、PhD
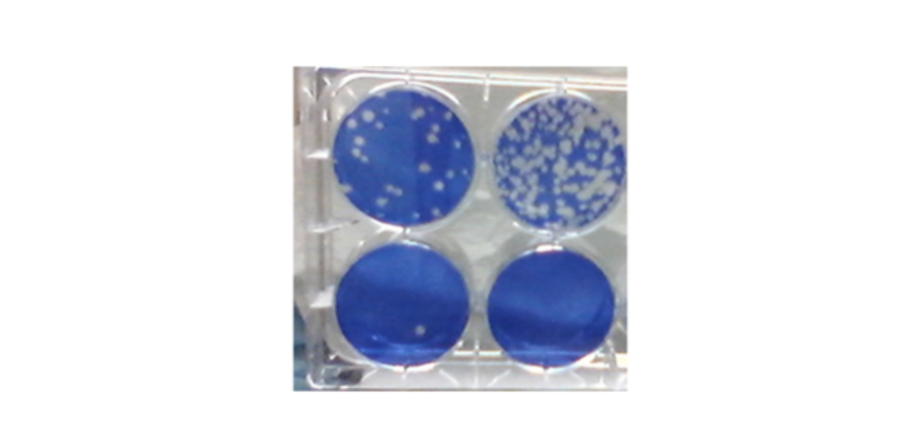
コロナウイルス複製の阻害を測定するためのSARS-CoV-2プラークアッセイ。 青い色は生細胞です。 穴は「プラークはSARS-CoV-2が細胞に感染して殺した場所を示しています。
写真提供者:Steven Bradfute、PhD
ハンタウイルスは、人間に深刻な病気を引き起こす危険な病原体です。 ウイルスは齧歯動物で無害に複製し、エアロゾル化した齧歯動物の排泄物でウイルスを吸入することで人間に感染します。 米国で最初の病原性ハンタウイルスであるシンノンブルハンタウイルスは、1993年にニューメキシコで発見されました。ニューメキシコでは、他のどの州よりもシンノンブルハンタウイルスの症例が最も多く、特に致死率が高いことから、この地域にとって重要なウイルスとなっています。人間の割合(〜35%)。 私たちの研究は、ハンタウイルスの生物学と治療法の複数の分野をカバーしています。
-治療薬用の中和抗体。
私たちは、アルバートアインスタイン医科大学を拠点とするNIH U19助成金の一環として、複数のハンタウイルスに対するモノクローナル抗体を特定および分析するための共同作業を行っています。 これらのデータは、コンソーシアムが抗体を選択して、小動物モデルを感染から救う能力をテストするために使用されます。 この共同研究は、「今週のウイルス学」ポッドキャストで強調されています:https://www.microbe.tv/twiv/twiv-578/
-シンノンブルハンタウイルス生存者における長期記憶免疫応答。
シンノンブルハンタウイルスの生存者における長期的な免疫応答を追跡しています。 現在までに、生存者に非常に強い抗体反応が見られ、感染後23人までの患者が依然として検出可能な中和抗体反応を示しています。 これらのデータは、ハンタウイルスの生存者が再感染に対して強力で長期的な免疫を生み出すことを示唆しています。 また、複数のメモリーCD13 +およびCD8 + T細胞コンパートメントで特定のハンタウイルスリコール応答をテストするために、4色フローサイトメトリーアッセイを確立しました。
-ニューメキシコの野生で捕獲された齧歯動物におけるシンノンブルウイルスの遺伝子分析。
シンノンブルハンタウイルスの宿主齧歯動物は、シロアシネズミPeromyscusmaniculatusです。 シカシロアシネズミは、米国のほぼすべて(南東部の地域を除く)で見られるため、非常に広い自然分布を持っています。 しかし、ヒトのシンノンブルウイルス感染は、主に米国西部と南西部に集中しています。 「なぜシカシロアシネズミはいたるところにいるのに、感染した人間はそうではないのか」という質問をしています。 ニューメキシコ州全体のヒト感染流行地域と非流行地域の両方で野生のシカシロアシを捕獲し、a)シンノンブルウイルスがヒト患者流行地域でのみ見られるのか、b)ウイルスゲノム配列であるのかを判断することで、この質問に答えています。地域によって大きく異なります。

Bradfute研究所は、2013年から2016年の発生時にジカウイルスを研究するために、新たなウイルス病原体に関する専門知識を活用しました。 私たちはロスアラモス国立研究所と協力して、ジカウイルス感染からマウスを保護する際の新しいDNA /ナノ粒子送達システムの有効性をテストしました。 新しいデリバリーシステムで処方されたプラスミドDNAワクチンが、用量依存的にマウスのジカウイルス感染に対する防御免疫を誘導することを発見しました。
Hraber P、Bradfute SB、Clarke E、Ye C、およびPitardB。ジカウイルスに対するDNAワクチンの両親媒性ブロック共重合体送達。 ワクチン36:6911(2018)

Bradfuteラボは、蚊媒介性であり、馬と人間の両方に重篤な疾患を引き起こす複数の脳炎ウイルスに対する交差反応性免疫応答の誘導のための新しいワクチンのテストに関与しています。
-広範囲に保護する単回投与のアルファウイルスワクチンのためのナノキャリア抗原送達。
私たちはLosAlamos National Laboratories(LANL)と提携して、複数のアルファウイルスに対する単発で長期的な免疫を提供する新しいDNAベースのワクチンをテストしています。 この共同研究における私たちの役割は、BSL-3アルファウイルスを標的として使用して、マウスにおける抗体およびT細胞応答の誘導についてDNAワクチンをテストすることです。
-ベネズエラ馬脳炎ウイルス感染における長鎖ノンコーディングRNA。
私たちは最近、ベネズエラ馬脳炎ウイルス感染に対する細胞応答における長鎖ノンコーディングRNAの役割を研究する大規模プロジェクトに対して助成金を授与されました。 このプロジェクトでは、UNM HSCの選択エージェントBSL-3施設を活用して、病原性ベネズエラ馬脳炎ウイルスのinvitroおよびinvivo感染後に、同じウイルスの非病原性バージョンと比較して、どの長鎖ノンコーディングRNAが発現するかをテストします。 このようにして、成功した細胞応答と失敗した応答でどの長鎖ノンコーディングRNAが誘導または抑制されるかを直接比較することができます。
エボラウイルスは、死亡率が40%を超える致命的な病原体です。 従来は孤立した村での小さな発生に限定されていましたが、ウイルスは初めて大都市に広がり始め、2013年から2016年にかけて世界的な発生を引き起こしました。 私たちは、このウイルスに対するワクチンと治療法の開発に取り組んでいます。
-エボラウイルスワクチンと治療法の開発。
ウイルス糖タンパク質のグリコシル化(糖パターン)の変化は、ワクチンとして使用した場合にこれらのタンパク質が免疫応答を誘導する方法に劇的な影響を与えることがわかりました。 グリコシル化のこれらの変化は、ワクチンがさまざまな細胞型で作られるときに発生します。 異なるワクチンに異なる細胞型が使用されているため、我々の発見は関連性がありました。
-エボラウイルス治療とワクチンの同時投与。
私たちのエボラウイルス研究は、XNUMX回目の助成金の最近の資金提供を受けて継続されており、長期ワクチンと一緒に短期治療薬を投与することがこれらの治療法の有効性にどのように影響するかを研究しています。 目標は、同時投与されたワクチンの長期的な保護を無効にすることなく、ウイルスに対する即時の保護のために両方の治療薬を与えるための最適なタイミングを決定することです

進行中のコロナウイルスのパンデミックの緊急性を考えると、BradfuteラボはUNMHSCでのBSL-3SARS-CoV-2ウイルスの研究を主導しました。 私たちは25以上の異なる学術および商業グループと協力して、SARS-CoV-2の治療法、ワクチン、不活化、基礎生物学、および患者サンプル分析を研究するために独自の専門分野を使用しています。
-回復期および急性のCOVID-19患者における中和抗体の評価。
Bradfuteラボでは、回復期の個人の血漿と、UNMHでの実験的治療として回復期の血漿を注入された急性COVID-19患者の血漿中の中和抗体価をテストしました。 テストしたすべての回復期の患者は、酵素免疫測定法(ELISA)で測定した場合、スパイク表面タンパク質に対する抗体価が陽性でしたが、生きているSARS-CoV-2に対する中和抗体のレベルは回復期の個人では非常に低かったため、抗体レベルを高めたり、レシピエントで進行している病気を改善したりしないでください。 この研究は、ELISAによる全抗体だけでなく、患者への注入前の抗体価の中和のために回復期血漿を事前にスクリーニングすることの重要性を強調しました。 また、TriCore Reference Laboratoriesと協力して、中和抗体価が、生ウイルスの使用を必要としない、商業的に使用されている単純で迅速な抗体検出アッセイと相関することを示しました。
-表面のSARS-CoV-2を不活化する方法。
ライブSARS-CoV-2を不活化するために、いくつかの化学的、熱、光、およびその他の方法をテストしました。 また、N95マスクを乾熱で除染する一般的に提案されている方法は、生きているSARS-CoV-2を排除するのに効果的ではないことも示しました。
-回復期のCOVID-19個体における縦断的抗体およびT細胞応答の分析。 私たちは最近、SARS-CoV-2感染からの回復後の患者の免疫応答を追跡するためにUNM HSCCTSCから資金提供を受けました。 私たちはこの作業のために承認されたIRBを持っており、現在、最大50年間、抗体とT細胞の応答を分析するために10人の患者を募集しています。 この作品は、COVID-19サバイバーがウイルスに対する免疫応答を持っている期間に関する重要な質問に答えます。
--SARS-CoV-2に対する小分子のinvitroスクリーニング。
私のSARS-CoV-2作業の主要な側面の3つは、BSL-XNUMX実験室での生ウイルスに対するinvitroでの有効性について小分子をテストすることに集中しています。 私たちは、UNM HSC、UNMメインキャンパス、および非UNM機関と協力して、抗ウイルス活性について薬をテストしてきました。 私の研究室では、多くの小分子をスクリーニングし、複製を強力に阻害する一握りの分子を発見しました。 この作業により、多くの助成金の提出と、準備中または提出された原稿が作成されました。そのサンプルを以下に示します。