
マッケンジー研究所は、記憶がどのように作られるか、神経活動のパターンがどのように形成され伝播するか、そして発作の広がりをどのように制御するかを研究しています。
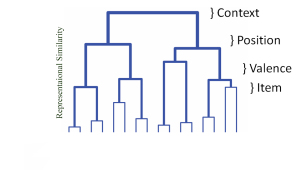
最も研究されている脳領域のXNUMXつであるにもかかわらず、海馬のコア機能は不明なままです。 私の仕事は リレーショナルメモリフレームワーク 海馬機能の。 この理論によれば、時間と空間で分離されたイベントは、海馬回路の連想リンクによって互いに関連している可能性があります。 この時空間ブリッジは、新しいルールとカテゴリの発見を可能にします。これは、このメモリシステムの主な機能と私は考えています。
どういうわけか、海馬は、そうでなければ弱い結合性を持っているであろう皮質領域を一緒に結合することができます。 機械学習の用語では、この海馬に依存するコヒーレンスは、学習が発生する可能性のある機能空間を拡張します。 詳細から規則性をどのように抽出するかに興味があります。 具体的には、私の研究室では、海馬/皮質の相互作用によって提供される拡張された特徴空間によって、カテゴリ学習がどのように影響を受けるかを研究しています。

生涯にわたって、1人に26人のアメリカ人がてんかんと診断されます。 利用可能な薬理学的治療は重大な副作用をもたらし、発作焦点の外科的切除などの代替治療を求める前に何年も苦しむことが多い人口の30%では効果がありません。 焦点が不明な場合、複数の病巣がある場合、または切除のリスクが高すぎる場合は、脳深部刺激療法が選択肢となる可能性があります。 現在、FDAが承認したXNUMXつのオプションがあります。 視床の前核の慢性的な刺激, 発作発症ゾーンに対する閉ループの「反応性」刺激。 これらの刺激プロトコルが効果的である理由、どの患者が最も恩恵を受ける可能性があるのか、またはいつどのように刺激するかを決定するための最良の戦略を誰も知りません。
私の研究室では、発作が始まる前に発作を検出する発作予測アルゴリズムの開発に取り組んでいます。 この高度な警告は、神経活動を混乱させて脳の同期を解除し、発作後の活動が発症ゾーンから健康な脳領域に広がるのを防ぐために使用されます。
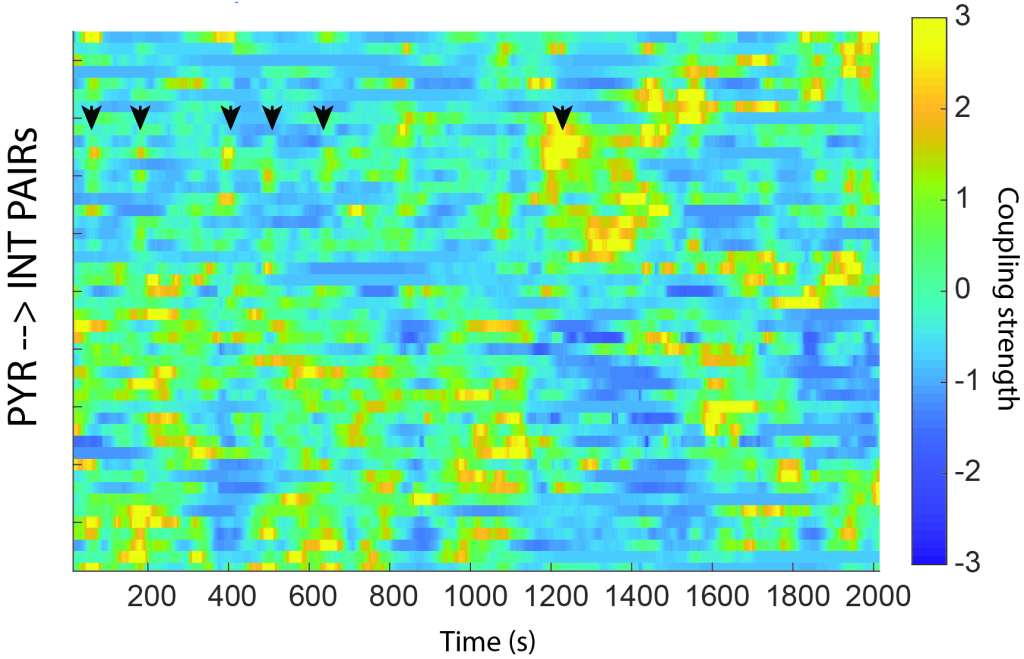
脳が自分自身と通信するために使用する神経活動の特徴を誰も知りません。 それは、どのニューロンが発火するか、それらのニューロンが特定の時間枠で発火する速度、ある時間枠内の同期活動のパターン、またはニューロンが相互に発火する順序でさえあり得る。 同期活動のパターンが重要であり、学習は、特定の状況でニューロンが一緒に発火する変化によってサポートされていると思います。 私の研究室では、興奮性ニューロンが互いにどのように競合して、短い時間枠で一緒に活動するかを研究しています。 私は、横方向の抑制における可塑性が、誰が誰と、どのような状況でそれらの共存の規則が適用されるかを決定する可能性があるかどうかを知りたいです。
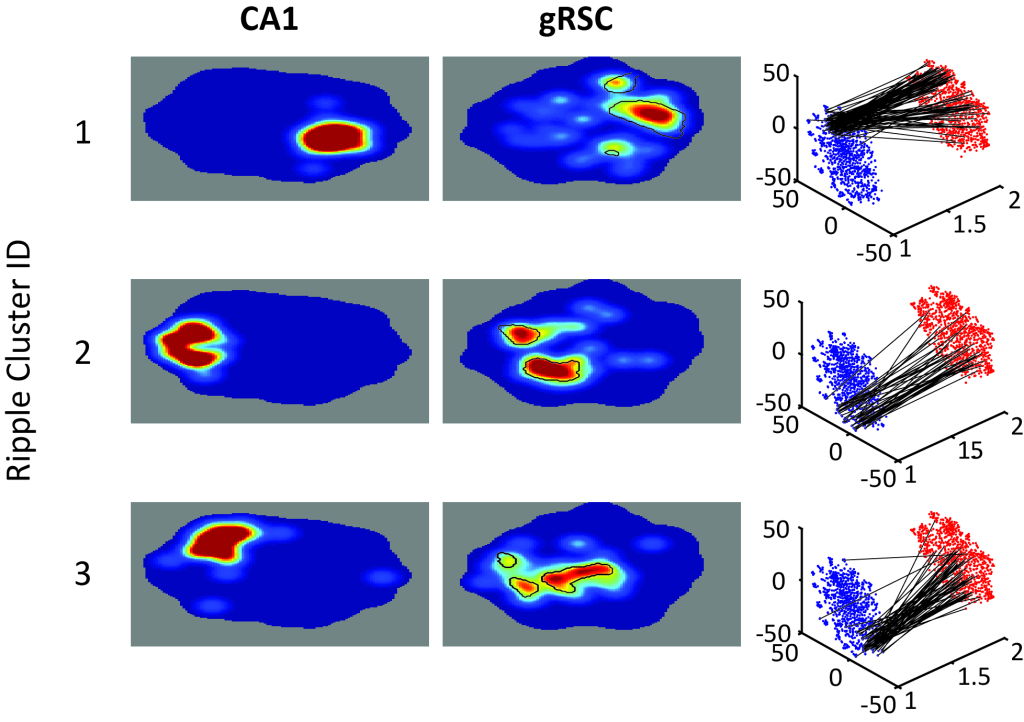
複雑な相関パターンと細かくバランスの取れた同期は、それらのスパイクが遠心性脳領域で発散活動を促進できる場合にのみ重要です。 同期アクティビティのパターンはどのように読み取られますか? 着信信号は、リージョン内の繰り返し接続を通じて出現した進行中のアクティビティとどのように相互作用しますか? これらの中央記憶回路の任意のシナプスでのシナプス伝達規則を理解するために、ある脳領域から別の脳領域の活動への入力の独自の寄与を切り離すことができますか?