ブリグマン研究室は、神経発達障害と精神神経疾患がどのようにして生活の質を低下させる不適応な行動変化を引き起こすのかを研究し、これらの欠陥を救済し、転帰を改善することを目的としています。

伝統的に、げっ歯類の研究では、げっ歯類の強み(穴を掘る、匂いを嗅ぐ、移動する)に焦点を当てた行動が利用されています。 これらのアプローチは豊富なデータをもたらしましたが、人間の認知機能を測定する方法とは大きく異なります。 この研究室の主な目標は、臨床データとより直接比較できる行動結果を調査するための新しいアッセイを開発して検証することです。 2001 年から、私は画面学習、記憶、および実行制御動作にタッチスクリーン アプローチを利用したタスクの開発と改良に取り組んできました。 この研究は、実行機能研究におけるマウスの有用性を確立するのに役立ち、ハイスループットスクリーニングのためのタッチスクリーンオペラントパラダイムの広範な採用につながりました。 過去 10 年間、私の研究室では、これらの作業中の皮質ニューロンの活動と局所電場電位の生体内記録を統合してきました。 in 生体 さまざまな脳領域が特定の行動をどのように媒介するかをより深く理解するのに役立ちます。 最近では、治療標的の開発におけるげっ歯類の行動データの有用性をテストするために、げっ歯類と人間の両方の特定の行動に関連する神経活動を比較する複数の大学の研究に参加しました。
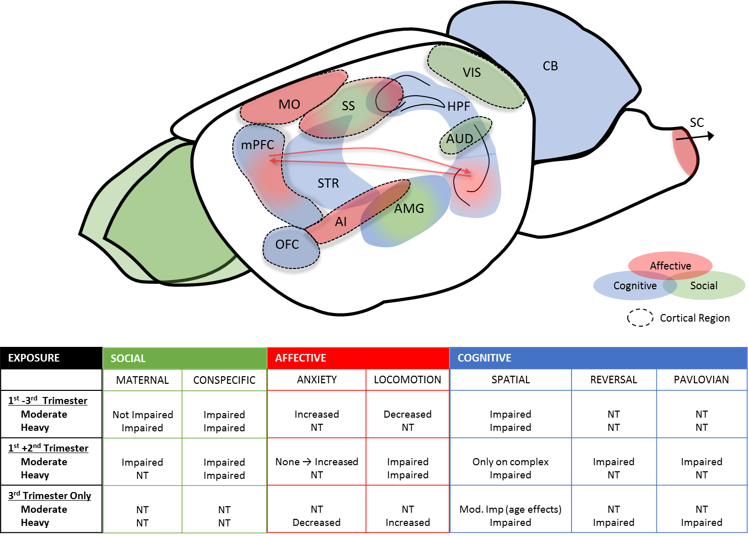
皮質機能とその根底にある実行制御プロセスに対するアルコールの影響は、これらの重要なプロセスの喪失が生活の質の大幅な低下につながる可能性があるため、重要な問題です。 発達期または成人の曝露が空間的課題、および程度は低いがオペラント課題に及ぼす影響は十分に文書化されているが、曝露後の回路レベルの変化を解析するために神経機能のオンライン測定を使用した研究はほとんどない。 テクニックを活用する インビボの 記録技術によれば、ブリグマン研究室は、より中程度の出生前曝露であっても、行動の柔軟性を損ない、皮質の発火と補充を変化させるのに十分であるとしている。 さらに、PAEは行動の柔軟性に必要な皮質-線条体の調整を調節不全に陥りました。 最近、我々は、PAEが成人初期までEtOHを断っていた場合の復帰行動と視空間識別も変化させることを示した。 興味深いことに、初期の人生の環境がこれらのモデルの結果を大きく変える可能性があることも示しました。
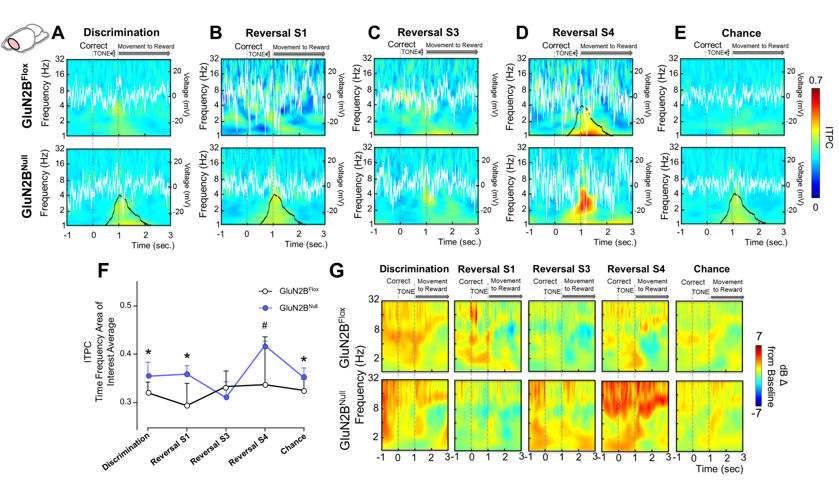
皮質、海馬、線条体における特定の NMDAR サブタイプの喪失は、学習とシナプス可塑性の両方を変化させる可能性があります。 ホームズ研究室で行われた基礎研究に基づいて、私の研究室は、前脳ワイドおよび条件付きノックアウトモデルと薬理学的不活化を使用して、NMDAR を含む GluN2A および GluN2B の役割を研究しました。 我々は、脳全体でGluN2Aが失われると、セットシフト課題における単純な学習と柔軟性が損なわれることを示した。 さらに、皮質と海馬における GluN2B の喪失により、識別学習は回避されるが、適切なルールを学習し、それらのルールを新しい問題に適用する能力は損なわれることを示しました。 より最近の研究では、GluN2B ノックアウトマウスと インビボの 行動中の記録は、サブユニットの喪失が皮質と層の両方の活動、および領域間のコミュニケーション方法を変化させることを示します。 出生前のアルコール曝露のような発達上の傷害がNMDARサブユニットの発現を変化させるという発見を踏まえ、我々は現在、この発現が効率的な学習と移行を媒介する可能性があるかどうかを調査している。
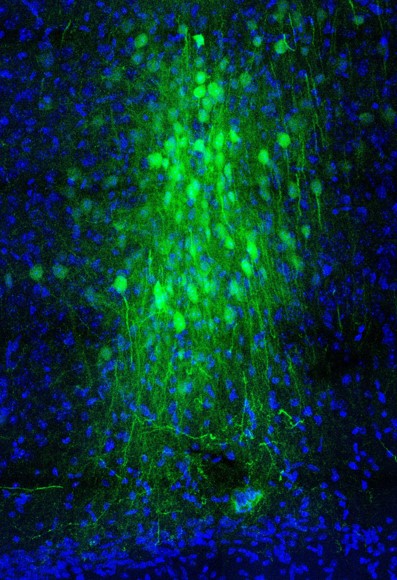
実行機能の障害は、多くの神経精神疾患の共通の特徴です。 実際、認知障害は、陰性症状や陽性症状よりも統合失調症患者の生活の質に大きな悪影響を及ぼす可能性があります。 統合失調症の前臨床モデルは、特定のシステムの喪失がどのようにトランスレーショナルタスクの行動障害につながるかを示しています。 以前、私は、前脳におけるGABA作動性機能の喪失は、注意力を変化させ、反転学習を損なうのに十分である一方、慢性フェンシクリジンは社会調査の尺度を変化させたが、学習と反転は免れたことを示した。 最近、ブリグマン研究所はUNMのメリオス研究所と協力して、 サーキュホーマー1a、前頭葉皮質で発現されるニューロンが豊富なcircRNAは、タッチスクリーン視覚識別タスクの逆転を妨げるのに十分でした。 重要なのは、メリオスの研究室が次のことも示したことです。 サーキュホーマー1a 統合失調症および双極性障害患者の PFC 組織の死後サンプルでは有意に減少しました。 現在進行中の共同研究では、環状マイクロ RNA の変化がどのように行動を損なうのかについてのメカニズムが研究されています。